يلعب دورا بالإصابة بالسرطان.. فوز أميركييْن بنوبل للطب لاكتشافهما الحمض النووي الريبوزي الدقيق
قالت الهيئة المانحة لجائزة نوبل -اليوم الاثنين- إن العالمين فيكتور أمبروس وجاري روفكون فازا بجائزة نوبل للطب لعام 2024 لاكتشافهما الحمض النووي الريبوزي الدقيق (ميكرو آر إن إيه) ومعرفة دوره في تنظيم الجينات.
وقالت جمعية نوبل في بيان صحفي إن الجائزة لهذا العام تكرم عالمين لاكتشافهما أن تنظيم نشاط الجينات هو أحد المبادئ الأساسية التي تحكم كيفية تنظيم نشاط الجينات.
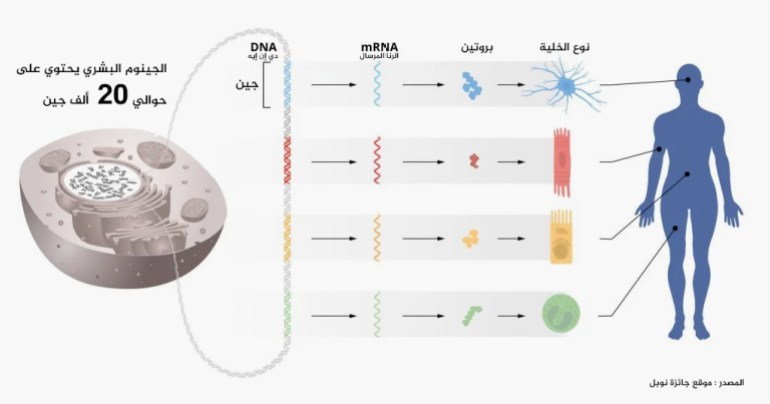
وأضافت أنه يمكن تشبيه المعلومات المخزنة داخل كروموسوماتنا بدليل التعليمات لجميع الخلايا في أجسامنا. وتحتوي كل خلية على نفس الكروموسومات، وبالتالي تحتوي على نفس مجموعة الجينات ونفس مجموعة التعليمات بالضبط. ومع ذلك، فإن أنواع الخلايا المختلفة، مثل خلايا العضلات والأعصاب، لها خصائص مميزة للغاية. فكيف تنشأ هذه الاختلافات؟ وتكمن الإجابة في تنظيم الجينات، والذي يسمح لكل خلية باختيار التعليمات ذات الصلة فقط. وهذا يضمن أن المجموعة الصحيحة فقط من الجينات نشطة في كل نوع من الخلايا.
وكان أمبروس وروفكون مهتمين بكيفية تطور أنواع الخلايا المختلفة. لقد اكتشفا الحمض النووي الريبوزي الدقيق (microRNA) وهي فئة جديدة من جزيئات “آر أن إيه” (RNA) الصغيرة التي تلعب دورا حاسما في تنظيم الجينات. وكشف اكتشافهما الرائد عن مبدأ جديد تماما لتنظيم الجينات والذي تبين أنه ضروري للكائنات متعددة الخلايا، بما في ذلك البشر. ومن المعروف الآن أن الجينوم البشري يشفر أكثر من ألف حمض نووي ريبوزي دقيق.
التنظيم الأساسي
تركز جائزة نوبل لهذا العام على اكتشاف آلية تنظيمية حيوية تستخدم بالخلايا للتحكم في نشاط الجينات. وتتدفق المعلومات الجينية من الحمض النووي إلى الرنا المرسال (mRNA) عبر عملية تسمى النسخ، ثم إلى الآلية الخلوية لإنتاج البروتين. وهناك، تتم ترجمة الرنا المرسال بحيث يتم تصنيع البروتينات وفقا للتعليمات الجينية المخزنة بالحمض النووي. ومنذ منتصف القرن العشرين، أوضحت العديد من الاكتشافات العلمية الأساسية كيفية عمل هذه العمليات.
وتتكون أعضاؤنا وأنسجتنا من العديد من أنواع الخلايا المختلفة، وكلها تحتوي على معلومات وراثية متطابقة مخزنة بالحمض النووي الخاص بها. ومع ذلك، تعبر هذه الخلايا المختلفة عن مجموعات فريدة من البروتينات. فكيف يكون هذا ممكنا؟ وتكمن الإجابة في التنظيم الدقيق لنشاط الجينات بحيث تكون المجموعة الصحيحة فقط من الجينات نشطة في كل نوع خلية محدد. وهذا يمكن، على سبيل المثال، خلايا العضلات، وخلايا الأمعاء، وأنواع مختلفة من الخلايا العصبية من أداء وظائفها المتخصصة. كما أنه يجب ضبط نشاط الجينات باستمرار للتكيف مع الوظائف الخلوية للظروف المتغيرة بأجسامنا وبيئتنا. وإذا حدث خطأ في تنظيم الجينات، فقد يؤدي ذلك إلى أمراض خطيرة مثل السرطان أو السكري أو المناعة الذاتية. ولذلك، كان فهم تنظيم نشاط الجينات هدفا مهما لعقود عديدة.
وفي الستينيات، تبين أن البروتينات المتخصصة، المعروفة باسم عوامل النسخ، يمكن أن ترتبط بمناطق محددة بالحمض النووي وتتحكم في تدفق المعلومات الجينية من خلال تحديد الرنا المرسال التي يتم إنتاجها. ومنذ ذلك الحين، تم تحديد الآلاف من عوامل النسخ، وكان يعتقد لفترة طويلة أن المبادئ الرئيسية لتنظيم الجينات قد تم حلها. ولكن عام 1993، نشر الحائزون على جائزة نوبل لهذا العام نتائج غير متوقعة تصف مستوى جديدا من تنظيم الجينات، والذي تبين أنه مهم للغاية ومحفوظ طوال التطور.
البحث على دودة صغيرة يؤدي لاختراق كبير
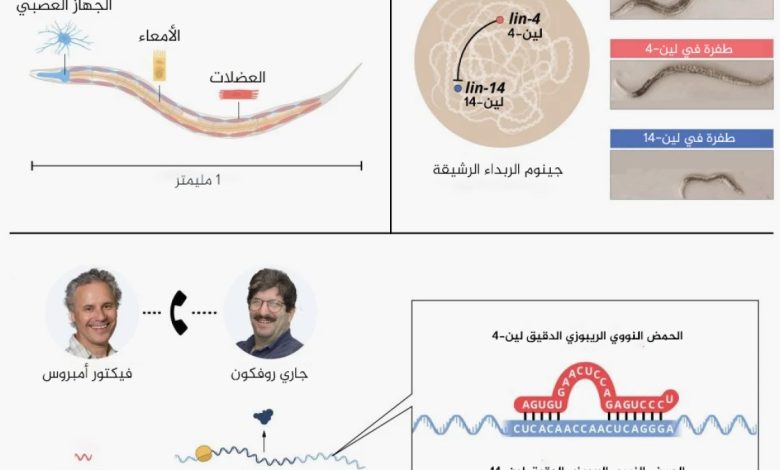
أواخر الثمانينيات، كان أمبروس وروفكون يعملان في مختبر روبرت هورفيتز، الذي حصل على جائزة نوبل عام 2002، إلى جانب سيدني برينر وجون سولستون. وفي مختبر هورفيتز، درسا دودة أسطوانية متواضعة نسبيا يبلغ طولها مليمترا واحدا، واسمها “ربداء رشيقة” (C. elegans).
وعلى الرغم من صغر حجمها، تمتلك دودة الربداء الرشيقة العديد من أنواع الخلايا المتخصصة مثل الخلايا العصبية والعضلية الموجودة أيضا بالحيوانات الأكبر حجما والأكثر تعقيدا، مما يجعلها نموذجا مفيدا للتحقيق في كيفية تطور الأنسجة ونضجها بالكائنات متعددة الخلايا. وكان أمبروس وروفكون مهتمين بالجينات التي تتحكم في توقيت تنشيط البرامج الجينية المختلفة.
وقد درس الباحثون سلالتين متحولتين من الديدان “لين-4″ (lin-4) و”لين-14” (lin-14) فأظهرتا عيوبا في توقيت تنشيط البرامج الجينية.
وأراد الفائزان بالجائزة تحديد الجينات المتحولة وفهم وظيفتها. وكان أمبروس قد أظهر سابقا أن جين “لين-4” يبدو أنه منظم سلبي لجين “لين-14”. ومع ذلك، لم يكن معروفا كيف تم حظر نشاط الجين الأخير. وكان أمبروس وروفكون مهتمين بهذه الطفرات وعلاقتها المحتملة وشرعوا في حل هذه الألغاز.
وقام أمبروس بتحليل الطفرة في جين “لين-4” في مختبره الذي تم إنشاؤه حديثا بجامعة هارفارد. وسمح رسم الخرائط المنهجي باستنساخ الجين وأدى إلى اكتشاف غير متوقع. وأنتج جين “لين-4” جزيء حمض نووي ريبوزي قصير بشكل غير عادي يفتقر إلى شفرة لإنتاج البروتين. وأشارت هذه النتائج المدهشة إلى أن هذا الحمض النووي الريبوزي الصغير من “لين-4” كان مسؤولا عن تثبيط “لين-14”. فكيف قد يحدث هذا؟
وفي الوقت نفسه، حقق روفكون في تنظيم جين “لين-14” بمختبره الذي تم إنشاؤه حديثا في مستشفى ماساتشوستس العام وكلية الطب بجامعة هارفارد. وعلى النقيض من الطريقة التي كان معروفا بها آنذاك أن تنظيم الجينات يعمل، فقد أظهر روفكون أن إنتاج الرنا المرسال من جين “لين-14” ليس هو الذي يتم تثبيطه بواسطة جين “لين-4”. ويبدو أن التنظيم يحدث في مرحلة لاحقة من عملية التعبير الجيني، من خلال إيقاف إنتاج البروتين.
وكشفت التجارب أيضا -عن جزء في الرنا المرسال الخاص بجين “لين-14”- أنه كان ضروريا لتثبيطه بواسطة جين “لين-4”. وقارن الفائزان بالجائزة نتائجهما، مما أدى إلى اكتشاف رائد، حيث تطابق تسلسل جين “لين-4” القصير مع التسلسلات التكميلية بالجزء الحرج من الرنا المرسال الخاص بجين “لين-14”.
وأجرى أمبروس وروفكون المزيد من التجارب التي أظهرت أن الحمض النووي الريبوزي الدقيق الخاص بجين “لين-4” يوقف جين “لين-14” عن طريق الارتباط بالتسلسلات التكميلية في الرنا المرسال الخاص به، مما يمنع إنتاج بروتين جين “لين-14”. وقد تم اكتشاف مبدأ جديد لتنظيم الجينات، بوساطة نوع غير معروف سابقا من “آر إن إيه” (RNA) وهو الحمض النووي الريبوزي الدقيق.
وقد نشرت النتائج عام 1993 في مقالتين في مجلة الخلية “سل” (Cell).

وفي البداية، قوبلت النتائج المنشورة بصمت مطبق من جانب المجتمع العلمي. ورغم أن النتائج كانت مثيرة للاهتمام، فقد اعتبرت الآلية غير العادية لتنظيم الجينات من سمات ديدان الربداء الرشيقة، وربما لا علاقة لها بالبشر والحيوانات الأخرى الأكثر تعقيدا. وقد تغير هذا التصور عام 2000 عندما نشرت مجموعة روفكون البحثية اكتشافها لجزيء الحمض النووي الريبوزي الدقيق آخر مشفرا بواسطة جين اسمه “ليت-7” (let-7).
وعلى عكس جين “لين-4” كان جين “ليت-7” محفوظا وموجودا في جميع أنحاء مملكة الحيوان. وقد أثار المقال اهتماما كبيرا، وعلى مدار السنوات التالية، تم التعرف على مئات من الحمض النووي الريبوزي الدقيق المختلفة. واليوم، نعلم أن هناك أكثر من ألف جين لجزيئات الحمض النووي الريبوزي الدقيق مختلفة في البشر، وأن تنظيم الجينات بواسطة الحمض النووي الريبوزي الدقيق مشترك بين الكائنات متعددة الخلايا.
أهمية عميقة
لقد كان تنظيم الجينات بواسطة الحمض النووي الريبوزي الدقيق، الذي كشف عنه أمبروس وروفكون لأول مرة، موجودا منذ مئات الملايين من السنين. وقد مكنت هذه الآلية من تطور الكائنات الحية المعقدة على نحو متزايد. ونحن نعلم من البحوث الجينية أن الخلايا والأنسجة لا تتطور بشكل طبيعي بدون الحمض النووي الريبوزي الدقيق.
وقال البيان الصحفي إن حدوث اضطراب في الحمض النووي الريبوزي الدقيق يمكن أن يساهم في الإصابة بالسرطان، كما تم العثور على طفرات في الجينات التي تشفر الحمض النووي الريبوزي الدقيق في البشر، مما يسبب حالات مثل فقدان السمع الخلقي، واضطرابات العين والهيكل العظمي.
وتؤدي الطفرات في أحد البروتينات المطلوبة لإنتاج الحمض النووي الريبوزي الدقيق إلى متلازمة “دايسر1” (DICER1) وهي متلازمة نادرة ولكنها شديدة الارتباط بالسرطان في مختلف الأعضاء والأنسجة.








